三、受照人群组的剂量
1. 概述
辐射剂量是辐射健康效应评估的重要依据。因此,UNSCEAR 2011年附件D中较详细地阐述了各受照人群组的辐射剂量,包括事故应急和善后工作人员以及一般公众的辐射剂量,后者分别考虑了事故后撤离人员,白俄罗斯、俄罗斯联邦和乌克兰污染地区的公众以及远离切尔诺贝利核电厂国家的公众。
需要指出,从一般意义上讲,剂量表示从给定照射吸收的辐射量,而剂量这个术语在UNSCEAR 2011年附件D中有2个具体的意义:表示物理量,即吸收剂量;表示防护量,即有效剂量。吸收剂量的单位是戈瑞(Gy),而有效剂量的单位是希伏(Sv)。通常,有效剂量的绝对值与吸收剂量有关。此外,也用到集体吸收剂量和集体有效剂量。
在UNSCEAR 2011年附件D中,甲状腺剂量以吸收剂量表示,单位为Gy;外照射和内照射造成的全身剂量以有效剂量表示,单位为Sv,这是辐射防护中用到的经过加权的量。为了进行比较,用到了天然本底辐射的世界年平均有效剂量2.4mSv,以及一次医学X射线断层扫描(CT)的典型有效剂量10mSv。
UNSCEAR 2011年附件D还指出,由于事故后在一定程度上采取了对策措施,使得辐射剂量相对较低(1986-2005年期间,3个共和国“污染地区”的平均剂量相当于CT扫描的剂量)。
与UNSCEAR 2000年报告相比,UNSCEAR 2011年附件D在受照人群组的剂量估算方面,有以下不同:(a)对于白俄罗斯、俄罗斯和乌克兰的大量善后工作人员,用510000人取代了380000人,并更新了剂量估算值;此外,增加了对于爱沙尼亚、拉脱维亚和立陶宛的善后工作人员给出的新资料。(b)对于白俄罗斯和乌克兰的撤离人员,更新了甲状腺剂量和有效剂量的估算值;对于俄罗斯的撤离人员,给出了新的资料。(c)甲状腺剂量和有效剂量的估算范围扩大了,从三个共和国的5百万人扩大到1亿人。(d)对于其他国家的居民,更新了甲状腺剂量和有效剂量估算值。
受照人群的早期剂量估算,以当时可以得到的测量数据为依据,同时用到了有关环境对策的谨慎假定以及有关的环境和剂量学参数。结果是,剂量往往被高估了。
摄入131I的甲状腺剂量评价基于事故后几周内进行的直接甲状腺测量,辐射探测仪放置在颈部。自UNSCEAR 2000年报告以来在甲状腺剂量学方面的努力一直集中在利用各种流行病学研究重建剂量,流行病学研究自2000年报告以后已经得到扩展或者已经开始。
对于未作直接测量的个人,只要其居住地区有许多人作了检测,也作了甲状腺剂量估算。这些估算基于对直接测量的那些人们重建的甲状腺剂量分布,以及所考虑个人的饮食习惯。此外,对于那些居住地区很少或没有事故后几周内进行甲状腺测量的人们,也进行了甲状腺剂量重建。其中用到了在可用131I或137Cs沉积、照射率数据和牛奶中的浓度与甲状腺剂量之间建立的相关关系。
白俄罗斯、俄罗斯联邦和乌克兰已经建立了外照射剂量估算的方法学,并已应用到污染区的人口。外照射造成的剂量基于:(a)三个国家对土壤照射率和放射性核素(尤其是137Cs)浓度所作的大量测量;(b)按照年龄、季节、职业和房屋类型进行室内和室外停留时间的人口调查。所用的辐射传输模型考虑城市地区和乡村地区的沉积放射性在环境中的行为。主要由摄入产生的内照射的剂量估算基于134Cs和137Cs的全身测量(可用时),但较多基于由测量到的食物中134Cs和137Cs浓度和有关消耗的基本假定估算的饮食摄入量。
在所进行的对照病例(未受照的病例)研究中得到的个人甲状腺剂量估算值的可靠性较差,这些研究中涉及的大量个人没有进行直接甲状腺测量。这些个人的甲状腺剂量是根据模型评价的。有关研究对象的居住历史和饮食习惯的资料是在访谈中获取的。
在地理相关研究(常称为“生态研究”)中,很难得到未指明个人的剂量(称为“组剂量”),这代表的是生活在一个具体地点(定居点、行政区或一个周的部分地区)的给定年龄组成员接受的平均剂量。定居点某个特定年龄组中个人的平均甲状腺剂量,可以根据足够人数体内甲状腺131I含量测定来获取,一般来说,不确定性最小。这是因为未知甲状腺质量对个人剂量不确定性的贡献小于平均剂量的不确定性。例如,在俄罗斯联邦,已经采用了重建定居点平均甲状腺剂量的官方方法。采用这种方法,对于俄罗斯联邦4个污染最严重地区(布良斯克、图拉、奥廖尔、卡卢加)的超过3500个定居点的6个年龄组计算了平均甲状腺剂量。它们发表在有关平均甲状腺剂量的一本参考书中,现在用于俄罗斯联邦的地理相关(生态)流行病学研究中。对于乌克兰的受照人口,也可以得到相似类别的甲状腺剂量估算值。
由于碘浓缩在甲状腺内,事故后最初几个星期中,饮用受到131I污染的新鲜牛奶的人群组的甲状腺吸收剂量,高于由天然辐射源对甲状腺产生的剂量;尤其是婴儿和儿童中,他们消耗的牛奶量按比例来讲高于成人。相反,铯的化学特性与钾相似,因此,相对均匀地分布在全身,事故产生的有效剂量与天然本底产生的剂量是可比的,或者还比天然本底辐射产生的有效剂量低得多。
表3-1给出最新的剂量估算的详细情况和结果,这是根据20多年来的经验和测量数据得到的。在下面的小节中给出各受照人群组的辐射剂量详情与分析。
表3-1 主要受照人群组剂量估算值的汇总
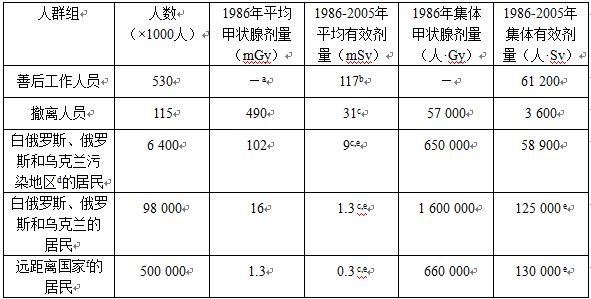
注:a. 只有少数的工作人员受到甲状腺剂量,因此,不可能对整个人群组给出可靠的平均值。
b. 工作人员的有效剂量估算值包括基本上在1986年至1990年受到外照射造成的剂量。假定记录到的mGy剂量在数值上等于以mSv表示的有效剂量。
c. 有效剂量估算值包括外照射和内照射贡献之和,不包括甲状腺剂量。
d. 在前苏联,污染区定义为土壤137Cs水平大于37kBq/m2。
e. 总剂量将继续累积,对于整个寿命期可能会增加25%。
f. 所有的欧洲国家,除了上述3个国家、土耳其以及高加索、安道尔和圣马力诺等国家。
2. 参与应急响应和善后工作的人群组
应急工作人员是参与事故应急响应的那些工作人员。第一天,大约有600个工作人员在现场从事应急响应,包括电厂工作人员、消防人员、保安人员和当地医疗机构的工作人员。UNSCEAR审查了这些受到非常高剂量的应急工作人员的资料,在其2000年的报告中指出:134个应急工作人员被诊断为急性辐射综合症,他们受到的全身(骨髓)γ外照射剂量介于0.8~16Gy。一些个人的皮肤剂量超过骨髓剂量10-30倍;一些个人接受的皮肤剂量估算为400~500 Gy。应急工作人员的剂量估算主要采用临床剂量学方法,即分析血细胞技术和/或血淋巴细胞的细胞遗传学参数,这些方法适合较少数量的研究对象,但不适合较大规模的流行病学研究。
善后工作人员是1986~1990年期间在电厂及其周围地区从事去污、建造石棺和其他善后工作(居民定居点去污等)的那些人员。那些在该核电厂其他机组工作的人员也包括在这个人群组中。在1986-1987年期间,大约440000个善后工作人员在切尔诺贝利现场工作,在1988-1990年期间,更多的善后工作人员加入了不同的工作。专门的健康登记系统给出,总共有超过500000个善后工作人员(表3-2中给出各国善后工作人员统计的总人数为526250人)。
善后工作人员的主要照射途径是沉积在地面和厂房表面的放射性物质的γ外照射。大约一半的善后工作人员的外照射剂量记录在国家登记系统内。只对有限数量的工作人员估算了β外照射对于皮肤和眼晶体的有效剂量和吸收剂量,以及内照射对于甲状腺的有效剂量和吸收剂量。此外,本小节还给出了善后工作人员集体剂量的估算值。
(a)γ射线发射体的外照射剂量
表3-2给出各相关国家登记系统记录的善后工作人员的外照射剂量统计情况。从表中可以看到,1986-1990年期间,善后工作人员受到外照射的平均有效剂量约为120mSv。在提供应急工作人员剂量资料的国家中,最高的平均剂量为150mGy,这是乌克兰工作人员受到的剂量,他们参与了切尔诺贝利现场早期最困难的操作,且在30km范围以内。最低的平均剂量(约为50mGy)是白俄罗斯的工作人员,他们没有被分配到工业区工作。俄罗斯善后工作人员研究指出,他们的平均剂量与其在第一次任务期间在现场花费的时间相对无关(表3-3)。这个表给出,大多数善后工作人员在第一次任务期间在现场花费的时间少于6个月。然而,一部分善后工作人员后来参与了多项任务,在现场的总时间达到几年。
表3-2 在国家登记系统中记载的善后工作人员外照射剂量a
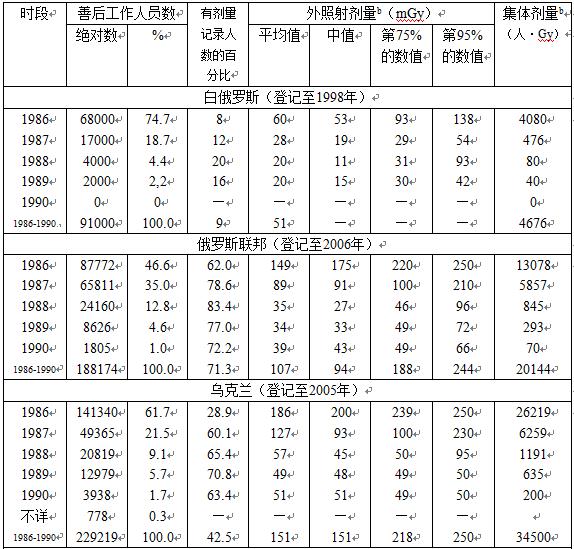
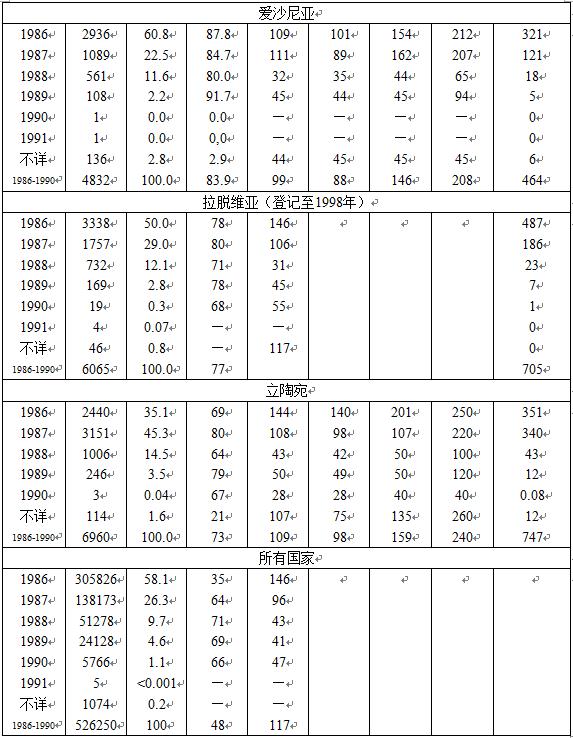
注a:为方便起见,外照射剂量表示为mGy。实际上,在许多情况下,测量到的是照射量。
b. 特定年份剂量分布的统计参数是按照有记录剂量的工作人员给出的(有记录剂量的百分比见表中第4列)。对于1986-1990年,给出的统计参数和集体剂量数值,基于假定有记录剂量的工作人员的剂量分布适用于所有的工作人员群体。对于某些人群,这个假定可能有疑问。
已经统计了白俄罗斯、俄罗斯联邦、乌克兰、爱沙尼亚、拉脱维亚和立陶宛的250000个有剂量记录的善后工作人员的外照射剂量分布。对于大多数国家,介于50-500mGy剂量段的工作人员数最多。剂量从小于10mGy至1000mGy之间变化,但85%以上的工作人员的剂量介于25-500mGy。对于219个工作人员,记录到大于1Gy的剂量,已经确认了这些工作人员剂量的可靠性。所有有记录剂量的工作人员的平均剂量为110mGy;各个国家的平均值是不同的,从白俄罗斯的43mGy至拉脱维亚的180mGy。
(b)β外照射对皮肤的剂量
估算了β辐射对无保护皮肤的剂量,比γ剂量高几倍。在面部高度测量了β+γ照射的总剂量率与单独γ照射剂量之比,结果是:从事一般去污工作的人员,为2.5-11倍(平均约为5倍);在3号反应堆中央大厅从事去污工作的人员,为7-50倍(平均约为28倍)。衣服屏蔽大部分皮肤,因此,受保护皮肤受到的β剂量比无保护皮肤小很多。
(c)内照射剂量
事故演变过程中在反应堆附近存在大量的131I和更短寿命的碘同位素,因此,那些事故后几周内在现场的善后工作人员可能因内照射接受很高的甲状腺剂量。根据1986年4月30日至5月7日进行的有限测量,估算了600个以上的工作人员的甲状腺剂量,平均值为0.21Gy,估算中假定在事故发生日单次摄入,且没有稳定碘保护。甲状腺剂量与有效剂量之比的中值估算为0.3。与1986年5月后的外照射剂量相比较,摄入131I产生的内照射剂量是可以忽略的。
在UNSCEAR 2000年报告中还提供了有关摄入90Sr、137Cs和239Pu产生的内照射剂量的有限资料。摄入这些核素造成的有效剂量负担的平均值估算为85mSv,这是对于约300个善后工作人员估算的,之所以在研究中选择这些工作人员,是基于他们受到高水平的外照射。
(d)集体剂量
在切尔诺贝利现场以及其他放射性核素污染地区工作并在国家登记系统内登记的善后工作人员大约有50万人,对于他们估算给出,1986-1990年期间由于外照射受到的集体剂量约为60000人·Gy。这些剂量中,73%是在1986年产生的,22%是在1987年产生的,其余的5%是在其后的3年中产生的。一半以上的剂量(56%)是由乌克兰人员接受的,33%的剂量是由俄罗斯人员接受的,其余11%的剂量是由白俄罗斯、爱沙尼亚、拉脱维亚和立陶宛的人员接受的。没有估算位于前苏联的其他国家的工作人员剂量。
此外,根据个人剂量水平也给出了白俄罗斯、俄罗斯联邦、乌克兰、爱沙尼亚、拉脱维亚和立陶宛的集体剂量分布以及合计情况。在所有有剂量记录的人员的集体剂量中,大约85%是由个人剂量介于50-500mGy的工作人员贡献的。
3. 事故后撤离的人群组
事故后,115000人从白俄罗斯、俄罗斯联邦和乌克兰污染最严重的地区撤离,主要在当年的4-6月,但也有在8-9月撤离的。其中,白俄罗斯约25000人,俄罗斯联邦约200人,乌克兰约90000人。人们撤离的区域成为“禁区”,不仅包括以切尔诺贝利反应堆为中心的30km范围的区域,还包括30km附近的高污染区和较远距离测量到高水平137Cs沉积的区域。
(a)甲状腺剂量
撤离人员接受的甲状腺剂量随他们的年龄、居住地、饮食习惯和撤离人员而变化。例如,普里皮亚季的居民基本上在事故后的40小时内撤离,人口加权的甲状腺剂量估算为370mGy,其范围从成人的275mGy至学龄前儿童的1000 mGy。对于白俄罗斯人口,估算给出很高的剂量,他们在1986年5月撤离,人口加权的剂量、成人剂量和学龄前儿童的剂量分别为1400、920和4600mGy(见表3-4)。对于全部撤离人员,人口加权的平均甲状腺剂量估算为490mGy,而白俄罗斯、俄罗斯联邦和乌克兰相应的数值分别为1100、440和330mGy。在表3-4中,可以看到,撤离人群中的学龄前儿童、学龄儿童和青少年的平均甲状腺剂量显著高于成人的数值。
表3-4 1986年从禁区撤离人群组的资料:人数、甲状腺剂量、集体甲状腺剂量
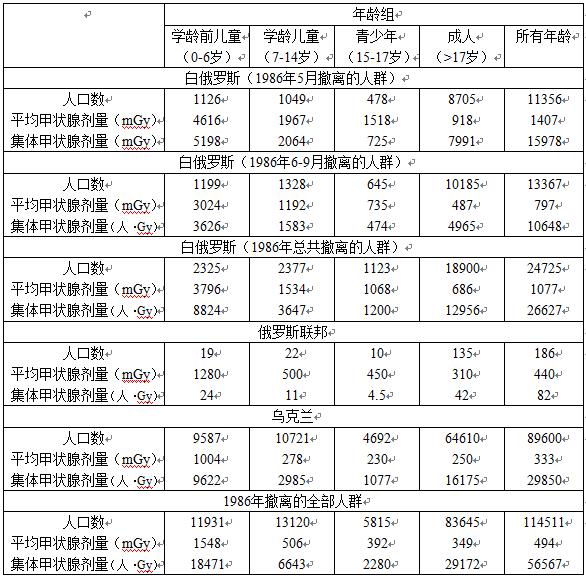
除普里皮亚季撤离人员以外,大多数撤离人员甲状腺剂量中占主导地位贡献者为消耗受131I污染的牛奶,其他核素和途径的贡献是很小的。摄入短寿命放射性核素(132I和133I)对甲状腺剂量产生最大贡献的是在事故后不久吸入放射性碘,并接着从污染地区撤离的那些人们;对这些人们,甲状腺照射占主导地位的途径是吸入。普里皮亚季居民在撤离前的1.5天内吸入了放射性碘,他们的身体计数数据分析指出,短寿命碘同位素对甲状腺剂量的贡献是非常大的。因此,对于那些不能或没有采取稳定碘预防措施(具体来说,口服KI片剂)的人群组,132I对甲状腺剂量的平均贡献估算为9%,133I的贡献为21%。总体来说,对于未服用稳定碘的人们来说,约30%的甲状腺剂量来自短寿命放射性碘。然而,对于在4月26-27日服用KI片剂的人们来说,贡献明显增加,即约40%来自132I,约14%来自133I。这样,在这个人群组中,一半以上的甲状腺剂量来自短寿命碘。此外,在这个组中,稳定碘预防措施减少131I对甲状腺剂量负担约一个量级,总的放射性碘产生的甲状腺剂量减少5倍。那些在撤离前多数时间待在室内的人们,平均接受的由131I产生的甲状腺剂量大约是大多数时间待在户外人们的二分之一。
(b)有效剂量
由外照射造成的(算术)平均有效剂量估算为:白俄罗斯撤离人员,约30mSv;俄罗斯撤离人员,约25mSv;乌克兰撤离人员,约20mSv。这些数值至少比由于内照射造成的甲状腺剂量的相应数值小10倍。由内照射造成的(算术)平均有效剂量估算为:白俄罗斯撤离人员,约6mSv;俄罗斯撤离人员,约10mSv;乌克兰撤离人员,约10mSv 。这些数值至少为外照射造成的有效剂量的二分之一。
(c)集体剂量
已经按各个剂量范围给出了甲状腺有效剂量的分布。对于白俄罗斯撤离人员,对甲状腺有效剂量的最大贡献来自大于5Gy的剂量类别;对于乌克兰撤离人员,最大的贡献来自0.2-0.5Gy的剂量间隔。对于全体撤离人员,对甲状腺有效剂量的最大贡献来自0.2-0.5Gy的剂量间隔。这两个国家撤离人员甲状腺的总有效剂量估算为约60000人·Gy。
对于1986年的撤离地区人口,总的有效剂量估算为约3600人·Sv。乌克兰人员在集体有效剂量中占有最大的份额,主要因为撤离的人数最多。
4. 白俄罗斯、乌克兰和俄罗斯联邦受影响地区的居民
在UNSCEAR 2000年报告中,特别关注了白俄罗斯、乌克兰以及俄罗斯联邦的污染区(137Cs沉积强度水平达到37kBq/m2)大约500万居民。在UNSCEAR 2011年附件D中,进一步对受影响地区(白俄罗斯和乌克兰的全部地区和俄罗斯联邦的19个地区)的全部人口估算了甲状腺剂量和有效剂量。总起来,大约1亿的人口。
(a)甲状腺剂量
与撤离人员的情况一样,对白俄罗斯、俄罗斯联邦和乌克兰居民甲状腺剂量占主导地位的贡献来自消耗含有131I的鲜奶。从表3-5中可以看到,与成人相比,学龄前儿童、学龄儿童和青少年受到较大甲状腺剂量的人数与相对百分比较高。图3-1给出估算得到的白俄罗斯、俄罗斯联邦和乌克兰儿童和青少年平均的和集体的甲状腺剂量。从中可以看到,三个国家受影响地区的儿童和青少年受到了较高的平均甲状腺剂量。
表3-5 白俄罗斯、俄罗斯联邦和乌克兰受影响地区人群甲状腺集体剂量的分布
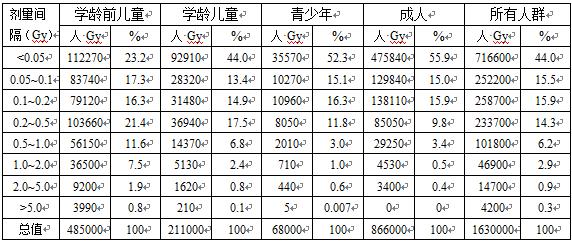
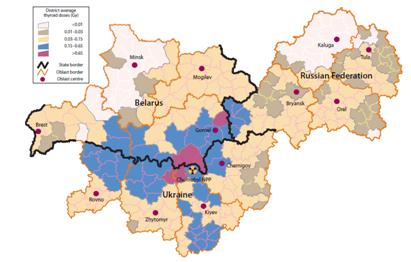
图3-1 估算的事故发生时白俄罗斯、俄罗斯联邦和乌克兰的儿童和青少年的平均甲状腺剂量
三个国家用来估算甲状腺剂量的方法有所不同,但所用的概念是相似的。方法基本上有两种类型:半经验方法;基于环境-迁移。很难融合它们来得到共同的方法。然而,国际癌症研究机构(IARC)进行了有限的比较研究,结果指出,所用的方法给出的结果有合理好的一致性,除低沉积密度地区以外。对于有大量人数在1986年5~6月作过体内甲状腺中131I活度直接测量的定居点,进行了平均剂量的比较,结果表明,白俄罗斯和乌克兰的剂量结果是高度一致的。靠近两国边界的白俄罗斯和乌克兰定居点的剂量估算值也是非常相似的。图3-5对于乌克兰608个定居点和白俄罗斯426个定居点给出1968~1985年出生的同期人群的平均甲状腺剂量。
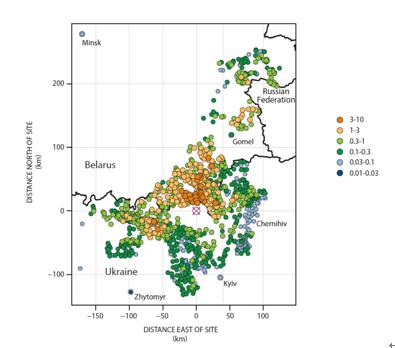
图3-2(图B-Ⅱ)
在UNSCEAR2011年附件D中还讨论了对甲状腺剂量的次要贡献,包括:摄入短寿命放射性碘(132I、133I和135I)和短寿命放射性碲(131mTe和132Te)产生的剂量;由地面和其他物质上的沉积放射性核素产生的外照射造成的剂量;摄入长寿命核素(例如,134Cs和137Cs)产生内照射造成的剂量。相关研究得出:
- 有关白俄罗斯儿童的研究指出,对于事故后几天内没有撤离的人群,短寿命放射性核素只有很小的作用。对于那些通过吸入途径摄入的人群,短寿命核素的贡献可以达到131I甲状腺剂量的20%;如果通过消耗污染食物途径摄入,则达到几个百分点的量级。
- 切尔诺贝利核事故后的外照射主要来自沉积的137Cs和其他相对长寿命的核素,它们以低剂量率产生外照射剂量,其中,对甲状腺剂量的贡献是多变的,大约分别占总甲状腺剂量中值和平均值的1.2%和1.8%。
- 在131I在事故后几周内衰变后,摄入当地生产的被137Cs放射性铯污染的食物成为内照射的主要途径。研究指出,摄入长寿命核素(主要是放射性铯)对甲状腺剂量的贡献通常小于3%。
(b)其他器官剂量和有效剂量
对于除甲状腺以外的其他器官剂量的主要贡献者是环境中的137Cs,其次是134Cs。134Cs和137Cs产生的外照射和内照射对于身体内所有器官和组织造成的剂量是相对均匀的。如前所述,内照射有效剂量不包括甲状腺剂量的贡献。估算的以mSv表示的有效剂量在数值上等于对体内任何器官(除甲状腺)的剂量(表示为mGy)。
对于白俄罗斯、俄罗斯联邦和乌克兰的大约一亿居民,估算了由内照射和外照射产生的有效剂量,3个国家各相关地区/州或城市居民的有效剂量数据均在UNSCEAR2011年附件D中详细给出。总的来说,事故后第一个20年中污染地区居民接受的由134Cs和137Cs产生的平均有效剂量估算为:内照射引起的,约为0.9mSv;外照射引起的,约为0.4mSv。
由于自1986年以来剂量是以不同的剂量率产生的,并将在未来几十年中继续产生剂量。对于污染区人口的估算给出,在外照射方面,典型的是,一生(考虑为相当于1986-2056年)有效剂量的25%来自1986年的辐射照射,1987-1995、1996-2005以及2006-2056年的相应数值分别为40%、15%和20%。与外照射相比,内照射剂量的较大部分是在1986年给予的,较少部分是在未来接受的。因此,内照射终身剂量的80%以上是在2005年以前给予的,不足20%的部分将在未来20年中以低剂量率给予。
(c)集体剂量
3个国家各相关地区/州或城市居民的集体甲状腺剂量和集体有效剂量数据均在UNSCEAR2011年附件D中详细给出。从地区水平来看,最高的甲状腺有效剂量位于高美尔州,160万人口受到了约320000人·Gy,相当于约200mGy的平均甲状腺剂量。然而,从国家的水平来看,对于乌克兰估算的甲状腺集体剂量是最高的,5100万人口中受到了约960000人·Gy,尽管乌克兰的平均甲状腺剂量估算值约比白俄罗斯低3倍。总起来看,对于3个国家考虑的9800万人口,甲状腺集体剂量估算为1630000人·Gy,大多数人们接受到小于0.05Gy的剂量,仅1%的人们接受的剂量大于2Gy。仅40%的集体甲状腺剂量是由污染区居民接受的,其余60%是由3个国家居民区(137Cs沉积密度小于37kBq/m2)接受的。如所预期的那样,平均甲状腺剂量随年龄而减少,学龄前儿童的剂量估算值比总人口估算值大2-4倍;估算给出,4%的学龄前儿童受到了大于0.2Gy的甲状腺剂量,0.005%受到了大于5Gy的甲状腺剂量。
1986-2005年的时间段中,3个国家中9800万人口接受的集体有效剂量估算为125000人·Sv;这个集体剂量的约二分之一是生活在137Cs沉积密度小于37kBq/m2地区的人口接受的。相应的1986-2005年的平均有效剂量估算为1.25mSv,约为1986年平均有效剂量估算值的3倍。对于总剂量的外照射和内照射组分,也观察到相差约3倍。就1986-2005年接受的有效剂量估算值而言,70%人口接受的剂量小于1mSv,20%人口接受的剂量介于1-2mSv。接受的剂量小于1mSv、介于1-2mSv和介于2-5mSv的那些人口的集体有效剂量估算为约占总有效剂量的20%。与甲状腺剂量情况相同,白俄罗斯的平均有效剂量估算值大于乌克兰或俄罗斯联邦,但乌克兰的集体有效剂量大于俄罗斯联邦(19个认为受影响的地区)和白俄罗斯,这主要由于乌克兰有较多的受照人口。
5. 远距离国家的居民
UNSCEAR在其1988年报告中根据未来环境传输模型的预测估算了北半球大多数国家的甲状腺剂量和有效剂量。其后,对于环境、食物和人体中的放射性核素水平,已经进行了大量的测量工作,包括旨在编制切尔诺贝利核事故后欧洲137Cs沉积地图集的大量努力。在此基础上,已经重新评估了大多数重要核素的沉积密度值以及所有欧洲国家(不包括土耳其、安道尔、圣马力诺和高加索共和国)人口的剂量估算值。
(a)甲状腺剂量
对于远距离欧洲国家的居民,重建甲状腺剂量的方法基于经由吸入和食入途径摄入放射性碘的评价。这与白俄罗斯、俄罗斯联邦和乌克兰用到的甲状腺剂量重建方法根本不同,后者主要基于1986年5-6月对体内甲状腺中131I的直接测量以及放射生态模式。基于摄入评价方法的估算值与基于人体测量的方法进行了比较,结果指出,前者通常系统地比后者给出较高的估算值和较高的不确定性。此外,基于经食入途径估算摄入量的剂量评价往往不考虑从世界上未受切尔诺贝利核事故影响的地区(例如从其他大洲)进口食物的贡献。这可能导致高估远距离欧洲国家的甲状腺剂量,在风险评估过程中需要考虑这些因素。
图3-3以地图形式给出学龄前儿童(0-6岁)甲状腺剂量估算值。在B3-3中,白俄罗斯、俄罗斯联邦和乌克兰的估算值基于人体测量法,而其他国家的估算值基于摄入评价法。甲状腺剂量估算值大致反映了137Cs沉积密度,但也受很多因素的影响,包括131I与137Cs的沉积密度比,放牧季节的开始,人们对新鲜牛奶的消耗,以及采取的应对措施。一般来说,甲状腺剂量主要是由摄入牛奶和新鲜蔬菜中的131I引起的。然而,对于那些在事故后不久就采取措施减少当地生产食品中放射性核素摄入的国家,吸入途径起着重要的作用,对于北欧的那些国家,情况亦然。
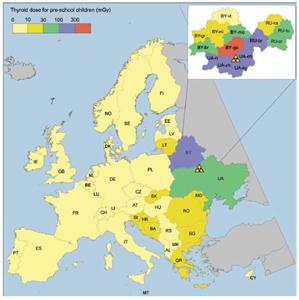
图3-3 事故发生时使欧洲学龄前儿童增加的平均甲状腺剂量分布图
(注:图中右上角是白俄罗斯、俄罗斯联邦和乌克兰相关州的分布图。图中BY-为白俄罗斯的州,UA-为乌克兰的州,RU-为俄罗斯的州)
如图3-3所示,白俄罗斯、俄罗斯联邦和乌克兰都至少有一个州的学龄前儿童的平均甲状腺剂量大于100mGy。在其他的欧洲国家,学龄前儿童的平均甲状腺剂量小于20mGy。在欧洲南部观察到甲状腺剂量介于10-20mGy,那里的放牧季节早于欧洲北部。
(b)有效剂量
已经利用标准程序估算了欧洲国家人口在1986-2005年期间由外照射和内照射产生的有效剂量。
外照射产生的剂量基于137Cs和其他γ核素沉积密度的大量测量值。采用的辐射传输模型考虑户外空气剂量率因放射性衰变而随时间减小,还考虑沉积放射性向土壤深层迁移。接着,由户外剂量率推算1986年接受的有效剂量,计算时对于乡村和城市人口分别用到了0.36和0.18的“行为”因子。对于后续几年接受的剂量估算值,乡村和城市人口的“行为”因子取值分别为0.31和0.16。
内照射产生的有效剂量分别按照吸入途径和食入途径进行估算。对于食入途径,考虑牛奶、奶制品、叶类蔬菜、其他水果与蔬菜和肉类的消耗。对大多数国家,1986年食物中137Cs的时间积分浓度及其消耗率取自UNSCEAR 1988年报告。137Cs的饮食摄入量(对1986年数值归一)随时间的变化,在一些国家中是相似的。估算中对于1987年和1988年分别用到了0.65和0.25的减缩因子;对于后续的年份,1989-1993年按照1.7年的半衰期指数衰减,1993-2005年按照7.3年的半衰期指数衰减。此外,来自保加利亚、捷克、芬兰、立陶宛和瑞士的当地专家提供各自国家的剂量估算值。
与甲状腺剂量估算的情况一样,大多数远距离欧洲国家的内照射有效剂量利用食物中放射性核素摄入模型估算。然而,与全身放射性计数法相比,这种方法可能显著高估内照射剂量,而全身计数方法能够直接评估合成放射性铯产生的内照射剂量。对于俄罗斯联邦的污染区进行了两种方法的比较,结果指出,采用摄入模型估算的内照射剂量高估实际摄入量2-3倍。尽管如此,在风险评价中还是可考虑这种对于远距离欧洲国家高估的内照射有效剂量。
图3-4给出对大多数欧洲国家估算的1986-2005年期间的总有效剂量。白俄罗斯、俄罗斯联邦和乌克兰的估算值基于全身计数法,而所有其他国家的估算值基于摄入模型推算。以mSv表示的有效剂量通常在数值上远小于学龄前儿童甲状腺的吸收剂量估算值(以mGy表示)。1986-2005年期间学龄前儿童甲状腺剂量与有效剂量的比值为:白俄罗斯、俄罗斯联邦和乌克兰,约为50;欧洲中西部国家,约为10;斯堪的纳维亚半岛,约为2或以下。这种不同部分是由于白俄罗斯、俄罗斯联邦和乌克兰采取了减少有效剂量的措施,而斯堪的纳维亚半岛较低的甲状腺剂量是由于放牧季节较晚开始。
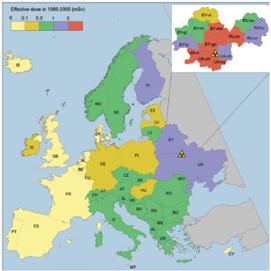
图3-4 1986~2005年期间事故使欧洲人口增加的有效剂量分布图
(c)集体剂量
在上述估算的甲状腺剂量和有效剂量基础上,采用1986年的人口数据(大约5亿人口),对于1986-2005年欧洲人口(不包括白俄罗斯、俄罗斯联邦和乌克兰,以及高加索、土耳其、安道尔和圣马力诺)估算的集体甲状腺剂量和集体有效剂量分别为660000人·Gy和130000人·Sv。1986-2005年期间相同人口的每人剂量为:甲状腺剂量,1.3mGy;有效剂量(不包括甲状腺剂量的贡献),0.3mSv。
四、切尔诺贝利核事故的早期健康效应
1. 概述
辐射照射的健康效应分成2类:
- 确定性效应,即在给定条件下肯定发生的效应,例如,在短时间内受到几个Gy照射的个人肯定会发生ARS(急性辐射综合症),这种健康效应也称为辐射照射的早期健康效应。
- 随机性效应,是可能发生或可能不发生的效应,例如,辐射照射的增加可能造成或可能不造成某个特定个人发生癌症,条件是这个特定个人所属的足够大的群体受到某个水平以上的辐射照射,在这个群体中的癌症发生率增加是可发觉的。这种随机性效应也称为辐射照射的晚期健康效应。
在这部分中介绍UNSCEAR有关切尔诺贝利核事故早期健康效应(确定性效应)的评估结论与相关的资料,有关该事故的晚期健康效应(随机性效应)的讨论给在第5部分中。
UNSCEAR 2011年附件D中指出,在评估健康效应时要考虑“归因”。所谓的“归因”是指将某个效应归因于某个特殊原因的过程。如果辐射照射不是某个特定效应的唯一已知原因,那么那个效应只是有可能以某个概率归因于辐射照射。
就“归因”而言,早期的确定性效应可较肯定地归因于辐射照射,这种效应至少要求怀疑受到在一个阈值以上的水平,通常是1Gy或更多的照射。同时,也要求在特定时间序列中观察到一组专门的临床或实验室结果。急性辐射综合征是确定性效应的很好例子,因为所观察到的症状和体征(例如骨髓中血液产生减少以及并发感染和出血,周边血液中染色体畸变的高发病率)不容易由其他原因所引起。尽管在确定诊断中有很大困难,但有经验的病理学家能将观察到的症状和体征归因于辐射照射。
有一些确定性效应,例如,白内障,辐射照射不是唯一的原因。如果这些确定性效应发生,通常是在高水平照射后的某些时间里;如果没有造成效应的辐射照射的具体标识,不太可能将效应肯定地归因于辐射照射,只是仅仅表示成辐射是效应的全部或部分原因的概率。
有关切尔诺贝利核事故急性的高水平辐射照射引起的早期严重健康效应,INSAG(国际核安全咨询组)在1986年8月就向国际社会提交了初步资料。临床资料分析给在UNSCEAR1988年报告附件D的附录“高剂量辐射对人的早期效应”中。UNSCAER2000年报告的附件J“切尔诺贝利事故的照射和效应”中给出了应急工作人员早期健康效应的更新资料。关于早期健康效应,UNSCEAR 2011年附件D中没有提出实质性的新资料,只是重述了已经明确得出的结论与相关的详细资料。
需要指出的是,UNSCEAR 2011年附件D中明确指出,急性辐射综合症病例发生在电厂工作人员和首批现场应急救援人员中,但没有发生在撤离的居民或一般公众中。在一般公众中没有ARS病例,不管是撤离人员还是未撤离人员。这与辐射照射估算是一致的。辐射照射估算表明,一般公众成员的全身辐射剂量远低于已知的ARS剂量阈值。
2. 事故应急工作人员中的急性辐射综合症
在事故后最初的几个小时中,许多ChNPP人员和消防员被当地医院确诊为有可能的辐射损伤综合症。几乎没有应急剂量测定。根据预期的辐射效应,似乎在爆炸的4.5小时内有150名受害者可能需要在莫斯科生物物理研究院的放射医学研究所得到深度治疗。
可能的急性辐射综合症最初考虑为237人。其中,115人转移到莫斯科生物物理研究院的放射医学研究所。几天内,这些人中确诊了104例ARS。之后,还经过回顾性验证确诊了34例,使得ARS的总病例数达到134。表4-1中给出这些患者的估算剂量和诊断结果。
表4-1 134个急性辐射综合症患者的有关数据
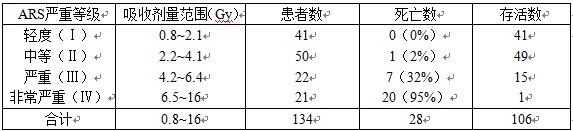
在不同严重程度的ARS患者的治疗中,澄清了骨髓综合症是主要的临床综合症。许多患者的骨髓综合症伴有皮肤辐射损伤;有些患者伴有角膜损伤(角膜炎)、肺部损伤(肺炎)以及肠道和口咽的损伤。
在最初的2天内进一步查明了皮肤的放射性污染以及摄入体内的核素(包括放射性碘和放射性铯)的放射性。相对于外照射吸收剂量,大多数患者由内照射引起的甲状腺剂量和肺部剂量是很小的。一些患者中,皮肤剂量超过骨髓剂量10~30倍,这些患者的估算皮肤剂量介于400~500 Gy。这种局部的皮肤辐射损伤显著加剧了已有的肺、肝或肾的异常。β照射产生的烧伤是若干患者死亡的主要原因,这显著增加了ARS的严重性。尤其是在皮肤烧伤超过全身表面积50%的情况下,是发病率和死亡率的主要起因。表4-2给出切尔诺贝利患者中ARS严重等级与皮肤烧伤和皮肤剂量的关系。
表4-2 切尔诺贝利患者中ARS严重等级与皮肤烧伤和皮肤剂量的关系
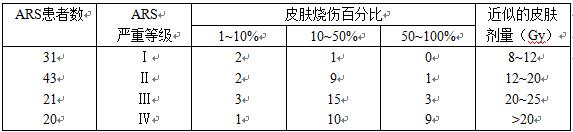
统计了28个ARS患者在事故后短期内死亡的情况,见图4-1。在早期(照射后14~23天),15个患者死于皮肤或肠道并发症,2个患者死于肺炎。在照射后的24~48天内,6个患者死于皮肤或肺部损伤,2个患者死于骨髓移植后的二次感染。一个患者患有ARS引起的急性弥散性间质性肺炎,并快速造成血氧不足而致命。2个患者在较晚时期(86~96天)死于与局部皮肤损伤以及肾功能不足有关的并发症。在最初的2个月中,底层骨髓衰竭是所有死亡的主要因素。
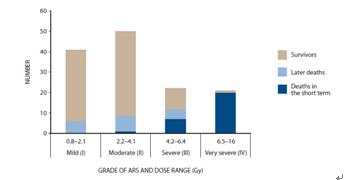
图4-1 ARS病人的最后结果
(尽管图中指出了每一类ARS晚期死亡的数字,但大多数这些病例不能归因于辐射照射。)
除了利用血球计数进行剂量估算外,也采用淋巴细胞培养计数。患者所受的准确剂量是很难估算的,因为估算基于一组临床症状,而基于骨髓抑制和细胞遗传的估算往往会得到不同的结果。对于I-II级ARS患者,一天进行两次生化和血液学指数测定;对于较严重的患者,进行每日评估。这些连续的计数对于选择支持治疗法和评估其有效性是十分重要的。细菌测定对于有效管理抗生素或抗真菌治疗也是重要的。
对于ARS患者,所采用的治疗方法包括:预防和治疗感染性并发症;解毒;肠外营养;输血疗法(同种异体骨髓移植和人类胎儿肝细胞注入);受损皮肤区的局部治疗;二次毒性代谢紊乱的纠正。
所有二级或以上的ARS患者安置在单独的房间,提供无菌的医疗管理。利用紫外线灯进行消毒,并要求医务人员彻底洗手,穿戴实验室外套和面具以及用无菌的解决方案洗鞋。每天更换患者的衣服。定期检测微生物污染指数。微生有机物保持在500个菌落数/m3以下。
这些患者接受内源性感染预防治疗,方法是利用发烧中的提炼物。对患者进行广谱抗生素静脉注射治疗,包括氨基糖甙类、头孢菌素和半合成青霉素。在一半以上的情况下,这种预防治疗通常能终止发烧。然而,如果在24~48小时小时内没有发生退烧,就对患者每12小时静脉注射4~6克丙种球蛋白。无环鸟苷第一次广泛而成功地应用于治疗急性ARS疱疹患者感染。大约三分之一的患者在脸、嘴唇和口腔黏膜上出现疱疹。
许多患者多次接受了捐赠的新鲜血小板输血。这些输血的疗效已得到证实,不仅长期(超过2~4周)血小板减少(低于5000~10000/)的患者没有危及生命的出血症,而且在大多数患者中也没有明显的出血增加迹象。平均来看,对于III级ARS的每个患者,3~5次血小板输血治疗是必要的。
红细胞输血对于治疗粒性白细胞缺乏的感染并发症不是必要的。然而,对于有显著损伤的II–III级ARS患者,需要进行红细胞输血。对于所有出现多器官损害的患者,采用现代解毒技术、抗感染和对症方法治疗。血吸收、血浆吸收和血浆置换得到应用。此外,直接抗凝也用来作为改善微循环的手段。肠道综合症治疗的主要特点是全肠道外营养加上用营养液和电解液来改进体液不足。这种治疗是十分有效的。
此外,对于高剂量(6~8Gy)的ARS患者,还进行了骨髓移植治疗。治疗时认为,在高剂量造成骨髓损害情况下,移植存活是可能的,但实际上,也发现移植的副作用以及移植物抗宿主疾病可能会对生命造成威胁
需要提及,在ARS幸存者中还遇到短暂周边血球减少、白内障、甲状腺疾病、局部皮肤损伤、神经心理障碍、肿瘤疾病等晚期健康效应。ARS幸存者的这些疾病分别在俄罗斯联邦的医疗生物物理中心(FMBC)或乌克兰的辐射医学研究中心(URCRM)进行专门的监护和治疗。
五、切尔诺贝利核事故的晚期健康效应
1. 概述
(1)影响随机性效应评估的因素
癌症是已在人群中证实的辐射照射的主要随机性效应。由于目前尚无手段来区别辐射诱发肿瘤与其他原因产生的肿瘤,基本上不可能将某个具体的癌症病例肯定地归因于辐射照射。另一方面,如果在受照人群中观察到癌症发生率(指这种疾病在一个规定时间里(通常为一年)发生的病例数)相对于未受照射人群(有相似年龄、性别、遗传素质、生活方式和其他相关因素)是增加的,而且如果这种增加与对其他受照人群得到的现有知识基础不是相矛盾的,就可以归因于辐射照射的增加,尤其是在所观察的发生率与剂量水平有关的情况下。
第4部分已经指出,早期的确定性效应可较肯定地归因于辐射照射,这是因为可以肯定地鉴别一个个体是否受到了阈值以上的辐射照射,以及是否已经在这个个体上观察到显著的临床结果。然而,随机性效应是在受到低剂量的群体中发生的,而癌症本身的诱发因素很多,有很多因素会影响癌症的发展与诊断,图5-1给出了这些影响因素的图解。因此,正确鉴别晚期的随机性效应,并给出可靠的归因分析,是正确认知切尔诺贝利核事故健康影响规模和性质的关键。与UNSCEAR 2000年报告相比,UNSCEAR 2011年附件D中作出了许多新的努力,不仅大大扩展了研究人群的范围,而且采用了科学的分析方法,并尽最大可能获取可靠的资料来源。
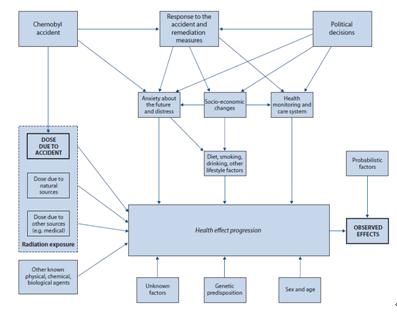
图5-1可能影响健康效应评估的某些因素图解说明
(2)长期健康效应评估的方法学
UNSCEAR 2011年附件D中指出,通常采用两种方法评价核事故的长期健康效应。第一种方法是采用由其他遭受辐射照射的人群推导出来的风险模型,例如,广岛和长崎原子弹爆炸幸存者,然后应用这些模型估算事故后相关人群接受的剂量,并预测这些人群的后续风险。第二种方法是对遭受事故照射的人群进行实证研究,以直接评价这些人群的健康效应。有关风险预测模型的应用在这一部分第4点中叙述,在这一部分第2点、第3点内容中则给出实证研究的结果。
实证研究方法的困难在于低的统计功效,这是因为相对低的剂量以及需要长期跟踪;然而,它的优点是直接考虑了受影响的群体。UNSCEAR 2011年附件D中将重点放在实证研究上,即直接对相关人群进行的那些研究,并优先考虑那些有精确的个人剂量估算值的群体。这些研究成为“分析研究”,可以对人体长期健康效应提供最直接的和最有说服力的证据。诸如剂量学、临床医学和病例解剖学等学科是这些分析研究的组成部分,有助于正确地解释观察结果。
通常,在评估受事故照射人群的癌症和非癌症发病率时,有两种类型的实证研究:
- 地理相关研究(通常也称“生态学研究”),这种研究按照所达到的年龄或诊断时的居住地来说明疾病发生率的特征。一项由较可靠风险估算进行的特定类型地理相关研究,已经用来分析切尔诺贝利核事故后的甲状腺癌风险。研究的病例与受照时的居住地有关,而且基于定居点的剂量估算,在这些居住地,已经进行了10人以上的剂量测定。
- 流行病学分析性研究,这种研究具有对照病例研究和同期群研究的特点。在这种研究中,混淆因素(如果是已知的,且是可以得到的)可以在个体水平上加以调整。然而,诸如科目选择或资料获取方面的偏差,可能是研究设计中的内在缺陷,不容易在分析中加以考虑。总体上,在辐射照射的可能贡献方面,认为分析性研究可以比地理相关研究提供较有利的证据。
UNSCEAR 2-11年附件D中还指出,在流行病学研究中,疾病的检查频度和诊断质量是十分重要的。理论上,这必需是与受照程度无关的,但在与切尔诺贝利核事故有关的流行病学研究情况下,特别要关注3个方面的问题:
- 对于受照群体采用了改进的诊断技术。尤其是,在切尔诺贝利核事故的研究中引入了超声技术检测甲状腺癌。与未受照群体相比,可能会增加甲状腺癌发病率的检出。
- 第二个问题是,专门的筛查计划使得有可能监测到已潜伏多年的小肿瘤。自切尔诺贝利核事故以来,在3个共和国中引入了若干正式的筛查计划,其中,甲状腺癌作为目标疾病,尤其是受到照射的儿童。有研究指出,这种专门的筛查计划会使检出的甲状腺癌发病率有几个百分比的增加。
- “疑诊偏倚”,是需要特别关注的第3个问题,即如果医生知道一个人受到切尔诺贝利核事故的辐射照射,并且认识到甲状腺疾病是可能的后果,那么,他或她可能已经倾向于作比原本更彻底的检查。
总体来看,解读切尔诺贝利核事故受照人群后果研究的结果,必须考虑检测方法随时间的变化,以及在高水平辐射照射人群和低水平辐射照射人员之间进行不同频度筛查检测的可能性。
(3)长期健康效应评估的资料来源
切尔诺贝利核事故长期健康效应评估的主要资料来源包括:切尔诺贝利登记系统和相关国家有关癌症发病率和死亡率的登记系统。尤其是,切尔诺贝利登记系统的数据与各国现有的死亡率和/或癌症发病率登记系统数据的连接,以及随后将受照人群的健康结果与相应的国家参考数据进行比较,被认为是流行病学研究的有价值工具。
切尔诺贝利核事故后,在全苏联开始了善后工作人员以及污染最严重地区居民的强制登记和健康监控,包括他们的后代。至1991年末,所有联盟的分散式临床-剂量登记处已经记录了659292人的信息。在苏联分解为多个独立的国家后,国家级的切尔诺贝利登记系统继续进行,但在每个国家是独立进行的。表5-1给出这3个国家中近500万登记者的最新数据。
表5-1(表D9)
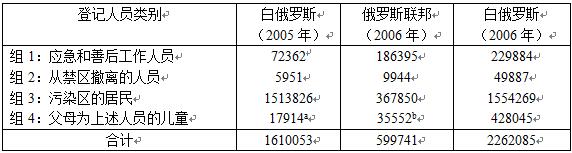
注a:以上3组人员出生的儿童。b. 仅是善后工作人员出生的儿童。
切尔诺贝利登记系统是评价切尔诺贝利核事故健康后果的一个重要资料来源。它们的主要优点在于,在前苏联的所有国家中,事故前和事故后都以系统的方式收集资料,而且,数据收集的准则是相同的。切尔诺贝利登记系统也有一些局限性,例如:由于登记与社会和经济利益有关,因此,已经提出了担忧,即这可能使得在所有这3个国家的登记系统中不适当地包含了大量的人数,因为在事故后20年,登记人数还在增加。又例如,早先的登记都是手工进行的,用于流行病学研究,需要使登记的数据实现计算机检索。
尽管如此,改善切尔诺贝利登记系统的努力一直在进行中。例如,1998年以后,一直努力建立“联合登记系统”来用于白俄罗斯和俄罗斯联邦受切尔诺贝利核事故辐射照射的那些人群,以有利于联合的流行病学研究,并增加他们的统计功效。在1998~2006年期间,在该联合登记系统内共有256000个应急善后工作人员及其43000个子女的资料。该登记系统还包括两个国家放射性污染最严重地区人群中甲状腺病例、白血病例以及乳腺癌病例的有关资料。
在流行病学研究中用到的一般公众的死亡率以及各种疾病的统计资料来自各国的国家登记系统。前苏联在1953年已经引入强制的癌症登记系统,所有新诊断癌症病例的有关资料都向病人所在居住地癌症登记处报告。上一世纪90年代初以后,已经作出努力来使现有系统计算机化,并且逐步改进它们的质量,以满足国际标准。1991年后,白俄罗斯已经建立了覆盖全国的癌症登记计算机网络。在乌克兰,已经有很先进的计算机化,预期很快覆盖全体人群。在俄罗斯联邦,仅在上一世纪九十年代末才开始计算机化。近几年中,3个共和国的重要登记系统发生了几个重大的变化。尤其是,2000年后,俄罗斯以及随后的乌克兰对于所有的公民和合法居民引入了通用的税务识别编码。这有助于通过地方的出生、婚姻和死亡登记办公室跟踪在切尔诺贝利登记系统中的登记者情况。
2. 甲状腺癌症的发病率
(1)儿童和青少年的甲状腺癌发病率
切尔诺贝利核事故中释放的131I和其他的短寿命碘同位素在白俄罗斯、俄罗斯联邦和乌克兰的许多地区对于甲状腺造成了很大的辐射照射剂量,这主要是通过饮用污染牛奶途径造成的。因此,甲状腺癌症的风险,尤其是在非常年幼的受照人群中的风险,是重要关切之一。在儿童中观测到的大量额外甲状腺癌症,明显成为这3个共和国中遇到的与辐射照射有关的重大公众健康问题。
儿童甲状腺是对电离辐射致癌效应最敏感的器官之一。自从切尔诺贝利事故以来,在三个共和国(白俄罗斯和乌克兰的全部地区以及俄罗斯联邦的4个最受影响的地区)的那些受照儿童和青少年中,甲状腺癌的发生率显著增加。在1986年未满14岁的人群中,1991-2005年期间报告了5127个的甲状腺癌病例。在1986年未满18岁的人群中,为6848个病例(在这些人群中,到2005年为止,15人死亡)。
表5-2分别给出白俄罗斯、俄罗斯联邦(4个最受影响的州)和乌克兰受照时18岁以下人群(儿童和青少年)中甲状腺癌发病率,它们按性别和不同的年龄给出。这些数据对应1982~2005年的时期,它们是由相应的国家癌症登记系统以及特定地区的专门切尔诺贝利登记系统给出的。图5-2以白俄罗斯为例给出受照时未满10岁儿童与1986年以后出生儿童的甲状腺癌发病率比较。
从表5-2中可以看到,在1991~2005年期间报告了较多的甲状腺癌病例,受照时18岁以下的人群中甲状腺癌的发病率显著增加,这种增加始于事故后4~5年,并且持续显现,所报告的甲状腺癌发病率可以达到每年每百万人几十例的水平(几十例/百万人/年),而从表5-2中也可以看到,事故前(1982~1985年)这个人群的本底甲状腺癌发病率很低(几例/百万人/年)。
图5-2说明,白俄罗斯在1986年切尔诺贝利事故后,受照时未满10岁儿童中的甲状腺癌发病率在1991~2005年期间显著增加。与表5-2的数据趋势相一致,女性的甲状腺癌发病率高于男性。对于1986年以后出生的儿童,没有证据表明甲状腺癌发生率增加,即使对他们增加了医疗监督。流行病学研究给出,这个地区未满10岁儿童中甲状腺癌的本底发生率为2-4例/百万人/年,而在图5-2可以看到,受照时未满10岁儿童的甲状腺发病率达到18~32例/百万人/年。
在几项对照组和同期群研究中已经证实了这种增加,而且这种甲状腺癌的过量增加与事故释放的放射性碘造成个人剂量的估算值是相关的。然而,这些研究的辐射风险估算值有一些不确定性,而且可能受到事故后采用各种超声检查和物理检查方法的影响。有研究指出,在白俄罗斯事故时为儿童和青少年的人群中, 60%甲状腺癌病例可能与辐射照射有关,其余的甲状腺癌发病例增加与加强监视、改进诊断技术以及其他的非辐射因素有关。
总之,受照时为儿童和青少年的甲状腺癌发病率的显著增加可归因于切尔诺贝利核事故的辐射照射。前面提到,当时的事故对策措施有缺陷,缺乏及时的通知,尤其是对私营农场主,因此未能控制131I污染牛奶的消耗。当然,这个发病率的显著增加,也会包括采用先进检测技术的贡献,因为与其他地区的同类人群相比,对于这个人群采用了较先进的超声检测技术。
表5-2 受照时18岁以下人群中的甲状腺癌发病率
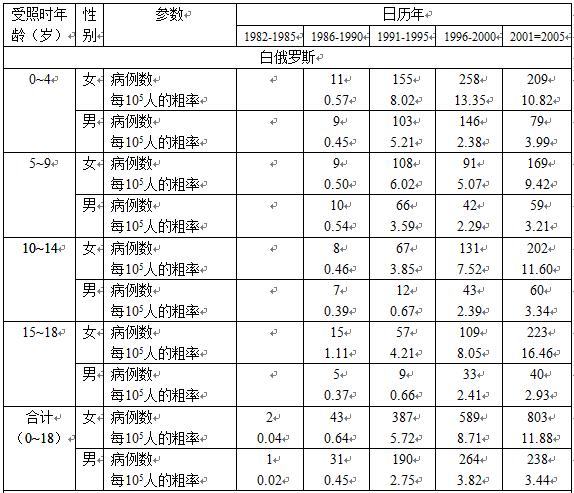
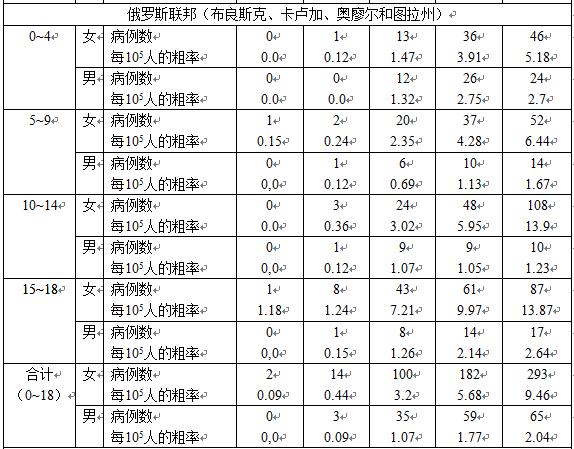
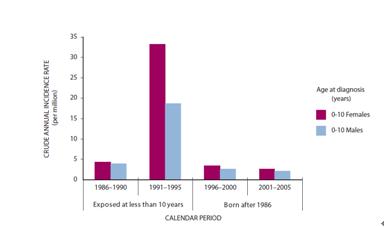
图5-2 白俄罗斯未满10岁儿童中诊断的甲状腺癌发生率
(2)成人的甲状腺癌发病率
儿童的甲状腺处于发育阶段,对于辐射照射特别敏感,因此,对于一个事故后几年得了甲状腺癌症以及事故时可能受到相对高甲状腺剂量的儿童,辐射照射引起癌症的概率可能是相对高的。然而,对于事故后几个月得了甲状腺癌症的成人,辐射成为诱因的概率是很低的,因为成人甲状腺对于辐射引起的肿瘤是非常有抗力的,肿瘤的发生相对于已知的照射和发病之间的最短潜伏期是非常快的。
在UNSCEAR2011年附件D中,主要关注两个人群组。第一组是污染区的撤离人员和居民,他们在事故后短期内主要受到了放射性碘对甲状腺的辐射照射。第二个关注的人群组是善后工作人员。除了那些在事故后最初几天内工作的人员(放射性碘对他们产生的内照射剂量是重要的)以外,善后工作人员接受的甲状腺剂量主要来自外照射,他们受到的外照射比一般公众受到的外照射平均剂量高得多。
对于上述两个人群组的甲状腺癌发病率,已经有大量的专项研究,但均未能得出切尔诺贝利核事故的辐射照射造成甲状腺癌发病率增加的结论。
例如,在俄罗斯联邦,已经对于放射性碘污染最严重的一个州——布良斯克州的居民报告了标准化的发病率比(SIRs)。与1991~1998年期间一般公众相比,布良斯克州的甲状腺癌发病率有统计意义上的超出。然而,对这些数据进行了剂量-健康效应分析,结果得出了负的剂量-健康效应的趋势。这种趋势表示剂量越高,风险越低。UNSCEAR 2011年附件D中指出:这个趋势提示,成人甲状腺癌发病率增加可能是增加筛查的结果,而不是由于辐射照射。
类似的情况也出现在善后工作人员的专项研究中。例如,在对俄罗斯的99000个善后工作人员中进行的研究中指出,甲状腺癌有明显的额外增加,但与辐射剂量没有联系。分析中考虑他们在30km范围内工作的时期,以及癌症是在潜伏期(1986~1991年)出现还是在后潜伏期(1992~1998年)出现。在潜伏期和后潜伏期都观察到明显增高的甲状腺癌发病率;在后潜伏期中的数值较高。然而,研究者得出,大多数的估算值给出与剂量的负相关关系。UNSCEAR 2011年附件D中指出,这些负的相关关系强烈地表示,到目前为止,善后工作人员受到的外照射剂量不是这个同期群甲状腺癌风险增加的重要因素,至少,筛查偏差是甲状腺癌发病率增加的部分原因。
3. 白血病和其他实体癌症的发病率
UNSCEAR 2011年附件D中,除了将重点放在甲状腺发病率以外,还研究了白血病、所有实体癌症等晚期健康效应,这是因为考虑到这些结果对于辐射的潜在敏感度。
(1)白血病
对于原子弹爆炸幸存者的研究指出,高剂量和高剂量率的电离辐射可以诱发白血病。此外,白血病是对电离辐射最敏感的癌症之一,而且这种癌症有最短的诱发期,大约在2年左右。切尔诺贝利核事故后,对于受照人群的白血病发病率开展了很多研究,研究的人群组包括:在子宫中受照的人群;儿童时受照的人群以及受照的成人。总的结论是,到目前为止,还没有有说服力的证据表明,在那些尚在子宫中受照的和儿童期受照的人群中有可量度的白血病风险增加。在善后工作人员群体中有可发现的效应,但还远未能得出明确的结论,即不足以将研究中得到的数据直接与高剂量和高剂量率(例如,原子弹爆炸幸存者)研究得到的风险值进行比较。
在UNSCEAR 2000年报告中已经给出几份地理相关研究,它们将在子宫中受照人群的白血病发病率与未受照人群作了比较。这些研究没有提供任何令人信服的证据说明可量度的关联。例如,一项研究对于乌克兰高污染区的在子宫中受照人群的累积白血病发病率与较低水平放射性地区的相应数值作了比较。研究中得到的病例数很少,估算出的白血病相对风险的置信区间较大,因此,不足以说明在子宫中受照人群的白血病与事故辐射有关联。又例如,英国内部发射源辐射风险检查委员会(CERRIE)评估了事故后婴儿白血病发病率的资料,然而,来自英国的数据太少,不足以得出坚实的结论。
在UNSCEAR 2000年报告中,也审查了若干有关儿童时受到切尔诺贝利核事故辐射照射人群的白血病发生率的地理相关研究。这些研究很少或没有提供由于辐射照射导致白血病风险增加的证据。自UNSCEAR 2000年报告以后,一些相似的地理相关研究比较了那些受照儿童中在事故前和事故后的白血病发病率,这些研究再一次没有提供证据来支持白血病风险在白俄罗斯、俄罗斯联邦或匈牙利有可量度的增加的假设。
除了地理相关研究外,还有关于受照儿童人群中白血病的分析研究(病例组-对照组研究)。例如,一项研究报告了在白俄罗斯、俄罗斯联邦和乌克兰3个共和国中进行的较大规模的病例组-对照组研究。这项研究给出混淆的结果:来自乌克兰的数据指出白血病风险与辐射照射有关联;来自白俄罗斯的数据指出两者之间没有重要的关联;来自俄罗斯联邦的数据指出两者之间没有关联。由于辐射剂量非常低(中值剂量小于10mGy),统计分析的功效减小。因此,研究报告得出结论,“这项研究没有给出令人信服的证据来说明切尔诺贝利辐射照射导致儿童白血病风险增加”。
至于受照成人白血病的发病率,包括了一般公众人群组以及应急和善后工作人员组。在UNSCEAR 2000年报告中指出,有几项有关切尔诺贝利核事故辐射受照成人白血病发生率的研究,而这些研究没有能提供有说服力的证据来说明有可量度的效应。在不同国家进行的大多数地理相关研究依赖于从国家登记系统得到的可用数据,它们没有提供令人信服的证据来说明白血病发病率增加。
对于应急和善后工作人员的白血病发病率,有较多的研究。尽管在有的研究中看到一些迹象,但均未能明确得出白血病发病率与所受辐射照射之间有相关关系。例如:
- 早期根据登记系统进行的病例组—对照组分析指出,对于那些1986~1987年在30km范围内工作的善后工作人员,在剂量与所有白血病例之间没有有意义的趋势。然而,在后续的研究中,1986~1993年之间总共诊断出36个非CLL白血病(CLL为慢性淋巴白血病,已经有这种病与辐射照射无关的结论)白血病例(病例数:对照病例数 = 1:3)。病例患者的平均剂量低于相应对照组的剂量,只是在最高剂量组中观察到了升高的(但不是有统计意义的)的相对风险。
- 在一项有关乌克兰大约175000个善后工作人员在1987~1993年之间的白血病发病率研究。研究中比较了在1986年受雇的第一组人员和1987年受雇人员(其时剂量较低)的白血病发病率。他们发现,第一组的白血病发病率大约是两倍,但没有研究得出这一组白血病发病率与剂量的相关关系。





 官网手机端
官网手机端

 微信公众号
微信公众号

 核能云端
核能云端